Gasdermin D(GSDMD)是经典和非经典炎症小体共有的关键下游效应蛋白。GSDMD被CASP-1,-4,-5和-11裂解后,释放其N末端结构域,该结构域在脂质膜上形成孔,最终导致细胞焦亡。
GSDMD (又名 DFNA5L 或 FKSG10 )属于成孔蛋白家族。人源的成孔蛋白家族家族有 6 个成员,
而鼠源的成孔蛋白家族有 1 0 个成员组成,包括GSDMA、GSDMB、GSDMC、GSDMD、GSDME和PJVK 。GSDMD在人体组织和不同的免疫细胞中广泛表达。此胞质蛋白具有两个不同的结构域,中间由一个连接区域分隔。C末端结构域会通过与N末端结构域(GSDMD-NT)结合而发挥自抑制功能。被激活后的经典或非经典炎症小体相关caspases会透过蛋白水解切割GSDMD的连接区域,从而释放出GSDMD-NT。这个功能性结构域会易位至质膜并寡聚化,形成内径约为18 nm的孔。这些膜孔允许可溶性胞质物(例如IL-1β和IL-18)以及非特异性离子(例如Na+流入和K+外排)的通过。
GSDMD孔在质膜上的积累会导致被称为“细胞焦亡”的程序性细胞死亡。这些坏死的促炎性细胞会显示出特征性的形态变化,例如细胞肿胀和形成气泡状的突出物,最终导致质膜破裂。PMR可以将胞内大分子释放出胞外,这些分子包括乳酸脱氢酶(LDH,为PMR的标准标记)和HMGB1。
GSDMD孔的形成是一个高度受控的过程。的确,避免不当或过度的细胞焦亡是非常重要,否则会导致许多病理性炎症的发生。在静止状态下,GSDMD的表达一般较低,在启动阶段时,其表达会受到转录调控。而直到被活化的CASP-1或CASP-11/4/5裂解前,GSDMD会一直处于自抑制的状态 。有趣的是,CASP-8也可以裂解并激活GSDMD,而CASP-3可以通过将GSDMD-NT裂解为非活性片段,来限制孔的形成。GSDMD-NT会优先靶向仅存在于质膜内部小叶中的脂质(磷酸肌醇),因此它只能从内部介导细胞死亡的发生。
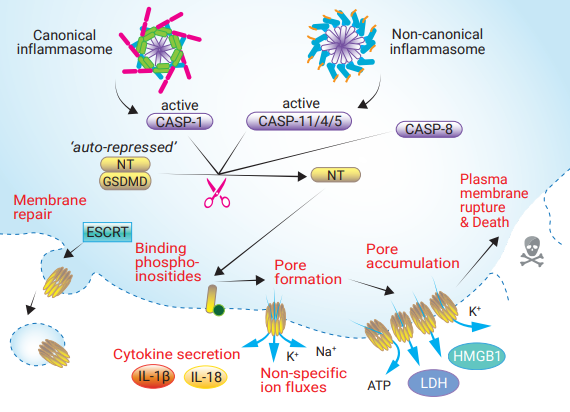
尽管GSDMD孔的形成通常会导致细胞焦亡,但有多种细胞类型(例如巨噬细胞,树突状细胞和嗜中性粒细胞)能够释放具生物活性的IL-1β并保持细胞存活。这些细胞利用由运输所需的内体分选复合物(ESCRT)-III机制介导的膜修复机制来预防或延迟细胞焦亡。这种机制通过泡吞作用吞噬受损膜来清除GSDMD孔。目前尚不清楚是否存在其他机制来分解或破坏GSDMD孔。
GSDMD已经成为一个具吸引力的药物靶点,以治疗人类各种炎性疾病。其他GSDM家族成员,例如GSDME和GSDMA3,也可能在人类疾病中发挥作用。未来如果对这些蛋白的机制和调控有更全面的研究,将有助开发靶向GSDM的治疗剂。
Gasdermin D细胞实验
监测GSDMD依赖性应答
THP1-KO-GSDMD Cells& RAW-ASC KO-GSDMD Cells
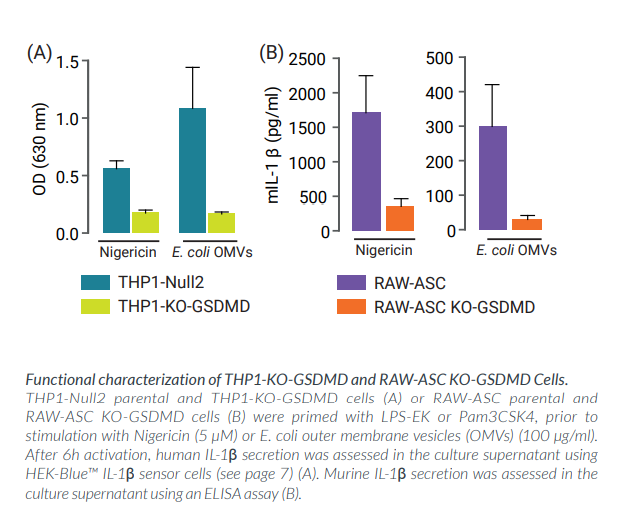
THP1-KO-GSDMD 和 RAW-ASC KO-GSDMD细胞分别来自人源单核细胞THP-1和鼠源巨噬细胞RAW 264.7并稳定表达ASC。这些细胞被敲除来双等位基因GSDMD的表达。它们在(例如使用Nigericin刺激的)经典炎症小体和(例如使用胞质LPS或OMVs刺激的)非经典炎症小体早期激活阶段时,表现出受损的IL-1β分泌和细胞焦亡。
更多详情请咨询Invivogen一级代理商-欣博盛生物
全国服务热线: 4006-800-892 邮箱: market@neobioscience.com
深圳: 0755-26755892 北京: 010-88594029 上海: 021-34613729
广州:020-87615159 香港: 852-69410778
代理品牌网站: www.neobioscience.com
自主品牌网站: www.neobioscience.net